张宏院士团队揭示自噬蛋白ATG-9调控溶酶体功能
近日,中国科学院生物物理研究所张宏院士团队在自噬研究领域取得重要进展,首次揭示了自噬关键蛋白ATG-9通过调控磷脂翻转酶活性,促进受损溶酶体修复的分子机制。该发现为溶酶体功能障碍相关疾病的治疗提供了新的研究方向。该篇题为"The autophagy protein ATG-9 regulates lysosome function and integrity"的文章于2025年4月9日发表在Journal of Cell Biology上。
ATG-9是定位于30-60 nm囊泡上的蛋白,在自噬体形成过程中的多个步骤中发挥作用。在酵母中,ATG-9作为"膜的种子"招募自噬机器,促进自噬膜的起始。同时,ATG-9具有促磷脂翻转酶活性,可调节膜脂质的不对称分布,影响膜形态和功能,从而促进自噬隔离膜的延伸。值得注意的是,ATG-9除了参与自噬过程外,哺乳动物中的ATG9A还参与协调ESCRT机器修复质膜损伤。张宏团队前期鉴定的新自噬基因epg-5的突变体中,自噬体和非降解自噬溶体大量积累,造成自噬底物的累积以及溶酶体轻度受损。张宏团队发现,在epg-5突变线虫中,ATG-9小泡可选择性聚集至轻度受损的溶酶体周围。令人惊讶的是,当ATG-9的促磷脂翻转酶活性减弱时,可显著促进轻度受损溶酶体的修复,并提高溶酶体活性,从而挽救自噬缺陷。
进一步研究表明,减少磷脂酰乙醇胺(PE)合成可产生与ATG-9磷脂翻转酶活性减弱突变体类似的表型。即在epg-5突变体中,降低PE合成同样能够促进溶酶体修复并改善自噬缺陷。这一发现表明,ATG-9的磷脂翻转酶活性减弱可能通过直接或间接地改变溶酶体膜内、外层磷脂的分布,进而影响膜曲率,促进溶酶体的生成和修复。
溶酶体功能受损及其完整性丧失与溶酶体贮积症及神经退行性疾病密切相关。本研究揭示的ATG-9磷脂翻转酶活性,为探索改善溶酶体功能障碍相关疾病的发病机制及其潜在的药物靶点提供了新的研究思路。
中国科学院生物物理研究所张宏院士为论文通讯作者,中国科学院生物物理研究所博士生彭康福为论文的第一作者。中国科学院生物物理研究所博士生赵国秀,副研究员赵红玉和北海道大学遗传病控制研究所研究员Nobuo N. Noda也参与了该课题的研究。本研究得到国家自然科学基金委,新基石科学基金会等机构的资助。

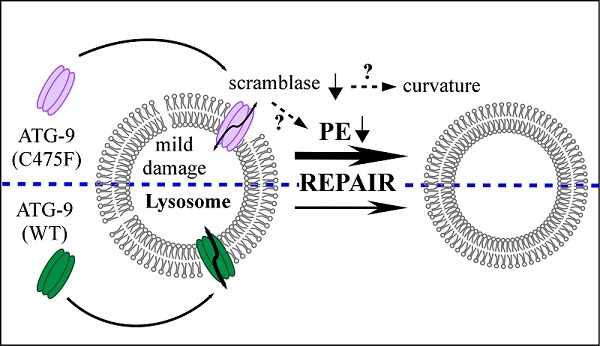 图 ATG-9参与损伤溶酶体修复的模型
图 ATG-9参与损伤溶酶体修复的模型
文章链接:
https://rupress.org/jcb/article/224/6/e202411092/277375/The-autophagy-protein-ATG-9-regulates-lysosome
(原标题:张宏研究组揭示自噬蛋白ATG-9调控溶酶体的功能)
特别声明:本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或者联系转载稿费等事宜,请与我们接洽。免责声明:本文为转载,非本网原创内容,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。
如有疑问请发送邮件至:bangqikeconnect@gmail.com